CARGA VIRAL E PERFIL DE RESISTÊNCIA AOS ANTIRRETROVIRAIS EM UMA POPULAÇÃO PEDIÁTRICA DO ESTADO DE SÃO PAULO EXPOSTA OU INFECTADA COM HIV-1
- Home
- /
- Blog
- /
- Resumo expandido TCC
- /
- CARGA VIRAL E PERFIL DE RESISTÊNCIA AOS ANTIRRETROVIRAIS EM UMA POPULAÇÃO PEDIÁTRICA DO ESTADO DE SÃO PAULO EXPOSTA OU INFECTADA COM HIV-1
Resumo expandido publicado nos Anais da III Mostra dos Trabalhos de Conclusão de Curso da Especialização em Vigilância Laboratorial em Saúde Pública. Para acessa-lo clique aqui.
Este trabalho foi escrito por:
Andressa Coelho Sichi¹; Cintia Mayumi Ahagon²; Valeria Oliveira Silva²; Luis Fernando de Macedo Brigido²
¹Estudante do Curso de Vigilância Laboratorial em Saúde Pública – NDSS – IAL; E-mail:
²Membros do Núcleo de Doenças Sanguíneas e Sexuais – Centro de Virologia, Instituto Adolfo Lutz
³Docente/pesquisador do Núcleo de Doenças Sanguíneas e Sexuais – Centro de Virologia, Instituto Adolfo Lutz
Resumo: A eliminação da transmissão vertical do HIV é uma das seis prioridades do Departamento de Doenças de Condições Crônicas e Infecções Sexualmente Transmissíveis (DCCI) do Ministério da Saúde, que ainda não foi alcançada. O teste padrão-ouro para diagnóstico do HIV-1 em crianças com menos de 18 meses de vida é a Carga Viral (CV), devido à permanência de anticorpos maternos. Para a identificação de resistência genotípica a região pol é a mais sequenciada por abranger as Classes de Antirretrovirais (ARVs) mais utilizadas: Inibidores de Transcriptase Reversa Análogo de Nucleosídeos (ITRN), Inibidores de Transcriptase Reversa Não Análogo de Nucleosídeos (ITRNN) e Inibidores de Protease (IP). A população deste estudo foi selecionada entre pacientes menores de 12 anos cujas amostras foram encaminhadas para o laboratório de Carga Viral no Centro de Virologia do Instituto Adolfo Lutz (IAL, São Paulo), entre 2018 à 2021. Para quantificação viral plasmática do HIV-1 foi utilizado o Abbott RealTime HIV-1 (Abbott, USA), para genotipagem foi feito o sequenciamento genético (Sanger). No estudo, foi considerado Transmissão Vertical (TV) 1.3% dos casos. Entre aqueles que estão sob Terapia Antirretroviral (TARV) à mais de 6 meses, 16/37% (43%) estão suprimidas virologicamente considerando <200 cópias/mL. Na genotipagem, 48% das sequências apresentaram ao menos uma mutação para ITRN, ITRNN ou IP. As mutações mais observadas foram M184V (16%) e K103N (16%); os ARVs com menor índice de susceptibilidade foram Nevirapina e Efavirenz. Programas que garantam o monitoramento da carga viral plasmática juntamente ao acompanhamento clínico devem ser instituídos ou aprimorados para promover a erradicação da transmissão vertical e obter o sucesso terapêutico à todas as crianças vivendo com HIV-1 à fim de alcançar a supressão viral.
Palavras–chave: carga viral; HIV-1; Terapia Antirretroviral de Alta Atividade; transmissão vertical de doenças infecciosas; técnicas de genotipagem
INTRODUÇÃO
Em 2020, estimava-se 1,7 milhão de crianças com idade entre 0 à 14 anos vivendo com HIV no mundo todo, onde 54% tiveram acesso à terapia antirretroviral (TARV). Cerca de 1,4 milhão de mulheres com HIV engravidam no mundo, se elas não receberem o tratamento adequado, a chance do vírus ser transmitido para o bebê varia de 15 a 45%. (UNAIDS, 2020; OMS, 2021). Contudo, esse índice cai para aproximadamente 1% caso a mãe e o bebê recebam a profilaxia com antirretrovirais no tempo e de forma adequada. A eliminação da transmissão vertical do HIV é uma das seis prioridades do DCCI e do Ministério da Saúde do Brasil. Ainda que essa prioridade apresente estatísticas otimistas ao decorrer dos anos, a meta ainda não foi alcançada. (BRASIL, 2019; Teshome et al., 2020)
Em 2008 a Organização Mundial da Saúde (OMS) revisou suas diretrizes e passou a recomendar início imediato da TARV após diagnóstico. Entretanto, a implementação do tratamento precoce requer o diagnóstico precoce, que pode ser inacessível em determinados ambientes devido ao custo mais elevado comparativamente aos testes convencionais, por exemplo os testes rápidos. Os testes de anticorpos comumente usados para adultos não podem ser utilizados devido à presença de anticorpos maternos que podem permanecer até os 18 meses de idade. O teste considerado padrão-ouro para crianças abaixo dessa faixa etária é a amplificação de ácido nucleico (Carga Viral Plasmática). (PENAZZATO et al., 2014)
Um dos principais fatores que leva às mutações é a baixa adesão à TARV, onde os pacientes não fazem o tratamento de forma adequada ocasionando a diminuição de ARVs circulantes na corrente sanguínea, consequentemente os níveis de fármaco não conseguem impedir a replicação do vírus. (VELOSO et al, 2010; BRASIL, 2019) A variabilidade genômica do HIV decorre principalmente da transcrição reversa do genoma do HIV, cujo evento é sujeito à erros. Durante a replicação do HIV, ocorre aproximadamente um erro a cada 10.000 nucleotídeos incorporados, e considerando que o genoma do HIV contém aproximadamente 10.000 nucleotídeos, estima-se que uma nova mutação é gerada a cada novo vírion produzido no organismo. (TAKEUCHI et al., 1991)
O gene pol é um dos genes estruturais do HIV, que contém 2.841 pares de base e 947 aminoácidos, e é responsável pela codificação das enzimas virais que atuam na replicação do vírus, sendo elas a Protease (PT), Transcriptase Reversa (RT) e Integrase (INT). A maioria dos sequenciamentos genéticos do HIV-1 são realizados para avaliação de testes de resistência genotípica, a pol é a região mais sequenciada para este fim, já que a maioria das classes de ARVs agem sobre estas enzimas. (RHEE, 2018)
Esse estudo tem como objetivos avaliar a taxa de viremia entre as crianças expostas ou infectadas com HIV-1 cujas amostras foram encaminhadas para o IAL entre 2018 à 2021 e avaliar os índices de mutações que conferem resistência às classes de ARVs dos ITRN, ITRNN e IP.
MATERIAIS E MÉTODOS
O projeto faz parte da pesquisa aprovada pelo Comitê de Ética em Pesquisa do Instituto Adolfo Lutz sob os seguintes protocolos: CTC-73D/2011 e CAAE: 02298012.6.0000.0059.
A população deste estudo foram os pacientes menores de 12 anos cujas amostras foram encaminhadas para diagnóstico ou monitoramento do HIV-1 ao Núcleo de Doenças Sanguíneas e Sexuais (NDSS) do Centro de Virologia – Instituto Adolfo Lutz Central (IAL), com solicitação do teste de Carga Viral e/ou Genotipagem no período de 2018 à 2021.
Para a Quantificação de RNA viral plasmático a extração foi realizada de forma automatizada pelo equipamento m2000sp (Abbott Molecular, EUA). Para a amplificação através do RT-PCR foi utilizado o produto final da extração no equipamento m2000rt (Abbott Molecular, EUA).
Para as extrações manuais de RNA foram utilizados os kits comerciais “QIAmp Viral RNA Mini Kit” (Qiagen, Alemanha)seguindo as especificações do fabricante. Após a extração foi realizada a amplificação da região Polimerase, dos genes da protease (PT) e transcriptase reversa (RT). O procedimento utiliza o método in-house pelo One-Step RT-PCR, combinando a retrotranscrição e amplificação, respectivamente. A etapa seguinte foi a amplificação de uma região interna do primeira amplificado envolvendo a PT e RT (Nested PCR). O protocolo utilizado in-house foi previamente descrito em trabalhos anteriores (SOLDI, 2019). Para confirmação da amplificação da região alvo foi realizada a eletroforese em gel de agarose à 1%.
Após a amplificação foi realizado o sequenciamento genético pelo método de Sanger, para revelar a composição nucleotídica. Foi adicionado o mix com nucleotídeos marcados com corante fluóforo e a placa foi levada ao termociclador Após a reação de sequenciamento, foi levada ao sequenciador automático ABI Prism 3500XL Genetic Analyzer (Life Technologies, EUA) por 25 ciclos de 96°C por 10 segundos, 50°C por 5 segundos e 60°C por 4 min.
A avaliação do grau de susceptibilidade aos ARVs foi feita por meio do algoritmo da plataforma de Stanford University HIV Drug Resistance Database – HIVdb (https://hivdb.stanford.edu/). Para isso, um score é revelado, sendo: alto nível de resistência, resistência intermediária, baixo nível de resistência, nível potencialmente baixo de resistência ou nenhum nível de resistência. (Stanford HIVdb, 2021)
As informações sobre quantificação de viremia plasmática (Carga Viral), quantificação de linfócitos T-CD4+ e tratamento foram obtidas através dos Sistemas de Informações do Ministério da Saúde: SISCEL (Sistema de Controle de Exames Laboratoriais) e SICLOM (Sistema de Controle Logístico de Medicamentos).
As variáveis utilizadas para análise foram qualitativas nominais e quantitativas (discretas e contínuas). Foram usados a mediana e Interquartil (IQR 25-75). Todas as estatísticas foram analisadas pelo software STATA version 14 (StataCorp LP, EUA).
RESULTADOS E DISCUSSÃO
Das 494 crianças analisadas, 447/494 (90%) foram encaminhadas para diagnóstico devido à exposição ao HIV-1. Dessas, 435/447 (97%) apresentaram CV Não Detectado (CV ND) no teste do IAL e apenas 14% têm dois testes de CV ND, seguindo o protocolo do Ministério da Saúde. (BRASIL, 2018)
Foi considerado Transmissão Vertical (TV) quando o teste do IAL foi a primeiro teste com quantificação superior à 200 cópias/mL e menos de 18 meses de vida, resultando em 6/447 (1.3%) de casos, taxa que reflete os levantamentos dos Boletins Epidemiológicos de 2019 e 2020, em que o Estado de São Paulo apresenta índices inferiores à 2%. É importante ressaltar que o índice ideal é a erradicação da TV do HIV-1 através de práticas voltadas à prevenção e profilaxia.
Para monitoramento da infecção do HIV-1 foram encaminhados 47/494 (10%) amostras; dessas, 13/47 (28%) têm resultado ND no teste do IAL porém apresentam viremia prévia e/ou histórico de tratamento. Existem 34/47 (72%) pacientes com coletas anteriores quantificáveis e que apresentam viremia no teste do IAL.
Diretrizes do Ministério da Saúde recomendam que a TARV deve ser iniciada o mais rápido possível após o diagnóstico. No estudo, 37 crianças fazem uso da TARV à no mínimo 6 meses, tempo suficiente para alcançar a supressão virológica. No critério proposto pelo CDC (2020) no qual é considerado supressão viral quando CV é inferior à 200 cópias/mL, temos 16/37 (43%) de crianças suprimidas. Esse índice indica falha na introdução e/ou adesão à TARV e no monitoramento, uma vez que a UNAIDS tenha proposto a meta 90-90-90. (UNAIDS, 2015)
Dezenove amostras foram parcialmente sequenciadas na região da pol (RNA). A mediana de idade em meses foi de 20 (4-77); a maior frequência foi do sexo feminino (79%) e 95% fazem uso de TARV. Em relação às mutações, 9/19 (48%) mostraram ao menos uma mutação para ARVs da classe de ITRN, ITRNN ou IP. Foi identificada a mutação V32L em 1/19 (5%), conferindo resistência Lopinavir e Darunavir. Para a classe ITRN, 26% apresentaram mutações de resistência, sendo a M184V (3/19; 16%) e T215S (1/19; 5%) as mais observadas desta classe. A mutação M184V, que também foi a mais observada no estudo de Mossoro-Kpinde (2017), confere resistência ou redução da susceptibilidade à Lamivudina e pode promover resistência de baixo nível ao Abacavir. Na classe dos ITRNNs, 42% apresentaram alguma mutação, a mais prevalente foi K103N (3/19; 16%), seguido da V108I (2/19; 10%). As características laboratoriais e demográficas dos pacientes que apresentaram mutações estão descritas no Quadro 1.
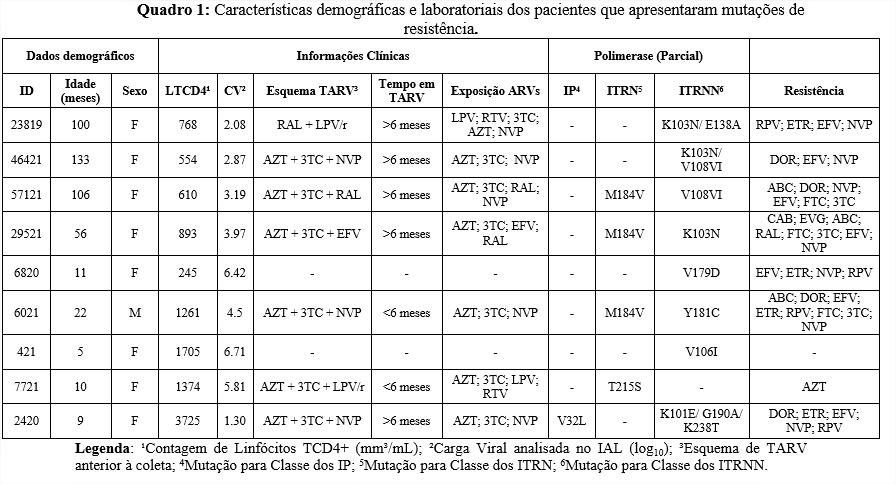
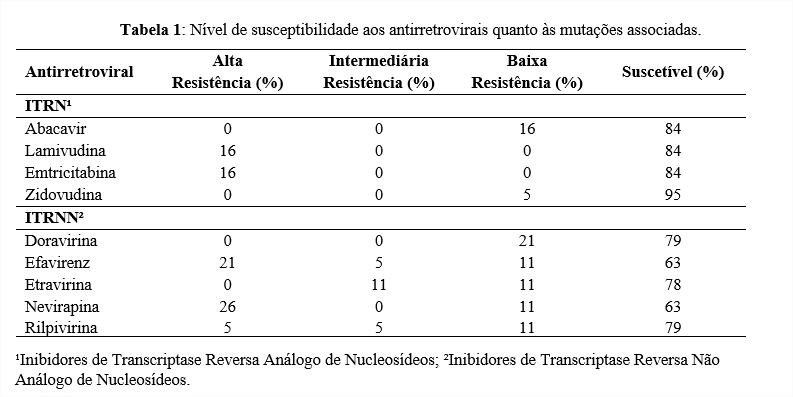
A K103N é uma mutação não-polimórfica e reduz a susceptibilidade à Nevirapina e Efavirenz, que foram os dois ARVs com os menores índices de susceptibilidade, como podemos ver na Tabela 1. (Stanford HIVdb, 2021)
Poucos estudos foram realizados a fim de avaliar a CV e as mutações de resistência em crianças. Houveram desafios envolvendo dados cadastrais e informações laboratoriais que de certa forma limitaram nosso estudo. Além disso, o número de amostragens nesse estudo foi pequeno, não sendo um referencial. As unidades de serviço parceiras do IAL pertencem à determinados municípios e apesar da demanda espontânea, esse trabalho pode não condizer com o cenário atual de todo o Estado de São Paulo.
CONCLUSÕES
Programas que garantam o monitoramento da carga viral plasmática juntamente ao acompanhamento clínico devem ser instituídos ou aprimorados para promover a erradicação da transmissão vertical e garantir o sucesso terapêutico à todas as crianças vivendo com HIV-1 com o intuito de alcançar a supressão viral. As taxas de transmissão vertical e supressão virológica, ainda que pareçam otimistas, não são ideais.
A observação de mutações de resistência e a diminuição na susceptibilidade aos antirretrovirais demonstra que a realização do teste de genotipagem pré-tratamento é fundamental para determinar a melhor escolha nos esquemas terapêuticos.
REFERÊNCIAS
UNAIDS. Global HIV & AIDS statistics – Fact sheet. UNAIDS, UNAIDS 2021 epidemiological estimates. 2021. Disponível em: https://www.unaids.org/en/resources/fact-sheet. Acesso em: 20 jan. 2022.
BRASIL. MINISTÉRIO DA SAÚDE. Manual Técnico para Avaliação de Exames de Genotipagem do HIV. Brasília, 2019a
BRASIL. MINISTÉRIO DA SAÚDE. Protocolo Clínico e Diretrizes Terapêuticas para Manejo da Infecção pelo HIV em crianças e adolescentes. Brasília, 2018
BRASIL. MINISTÉRIO DA SAÚDE. Protocolo Clínico e Diretrizes Terapêuticas para Prevenção da Transmissão Vertical de HIV, Sífilis e Hepatites Virais. Brasília, 2019b
MOSSORO-KPINDE, C.D. et al. Escalating and sustained immunovirological dissociation among antiretroviral drug-experienced perinatally human immunodeficiency virus-1-infected children and adolescents living in the Central African Republic: A STROBE-compliant study. Medicine (Baltimore). Hagerstown, 22 Mai 2020
RHEE S.Y. SHAFER R.W. Geographically-stratified HIV-1 group M pol subtype and circulating recombinant form sequences. Scientific Data. 31 Jul 2018
SOLDI, G. F. R. Avaliação da resistência aos inibidores da protease em pacientes vivendo com HIV em falha terapêutica. Dissertação (Mestrado em Ciências) – Secretaria de Estado da Saúde de São Paulo, Programa de Pós-graduação em Ciências da Coordenadoria de Controle de Doenças. São Paulo, 2019.
TAKEUCHI Y. et al. Low fidelity of cell-free DNA synthesis by reverse transcriptase of human immunodeficiency virus. Molecular Diversity Preservation International Multidisciplinary Digital Publishing Institute. Baltimore, 1988
TESHOME G.S.; MODIBA L.M. Strategies to Eliminate Mother-to-Child Transmission of HIV in Addis Ababa, Ethiopia (Qualitative Study). HIV/AIDS: research and palliative care. Auckland, 2 Dez 2020
VELOSO A.C.R. et al. Resistência genotípica do Vírus da Imunodeficiência Humana tipo 1 aos antirretrovirais. Com. Ciências Saúde. Brasília, 21(1):49-60. 03 Ago 2010
World Health Organization. Global Health Observatory data. Estimated antiretroviral therapy coverage among children. 10 nov. de 2021. Disponível em: https://www.who.int/data/gho/data/indicators/indicator-details/GHO/estimated-percentage-of-pregnant-women-living-with-hiv-who-received-antiretrovirals-for-preventing-mother-to-child-transmission. Acesso em: 20 jan. 2021.
World Health Organization. Global Health Observatory data. Estimated percentage of pregnant women living with HIV who received antiretrovirals for preventing mother-to-child transmission. 10 nov. de 2021. Disponível em:https://www.who.int/data/gho/data/indicators/indicator-details/GHO/estimated-percentage-of-pregnant-women-living-with-hiv-who-received-antiretrovirals-for-preventing-mother-to-child-transmission. Acesso em: 20 jan. 2021